1级乳腺癌存活_1级乳腺癌存活多久
1.乳腺癌WHO怎么分级
先和你简单的说一下概念上的问题:
乳腺癌的(组织学)分级: 是根据肿瘤组织的组织形态学进行分级,目前分为1-3级,1为分化良好,预后相对好,3为分化差,预后相对差。(举个可能不太恰当的例子去理解,如果把肿瘤当成一只敌人的部队,那组织学分级就说看敌人的装备情况,1级可能是大刀长矛,3级可能是导弹。需要注意的是目前我们对组织形态学的了解尚不足以准确预测肿瘤的恶性程度,这只是有一定的提示作用)
乳腺癌的分期(0,I-IV期):是根据肿瘤的大小,侵犯范围,淋巴结转移及是否远处转移来评价肿瘤在全身发展的阶段,并以指导治疗,及预测病人的预后。0期预后最好,IV最差(同样用上面的例子,乳腺癌的分期像是评价敌人的人数,占领的地方,是否已经占领了我们的敌后)。
可见,分期和分级是两个独立的指标。
根据你提供的情况,肿瘤组织学分级为II级,病理分期为IIb期(非常接近IIIa,因为肿块的大小是5cm,临界)。目前的化疗方案是很标准的方案,现在的反应是化疗引起的,化疗后可缓解。此后我推测医生会建议放疗及内分泌长期治疗。
乳腺癌是治疗手段比较多,预后较好的肿瘤,我觉得到目前为止你的治疗很标准,还是应该多听医生根据你具体的情况的建议,祝好运。
乳腺癌WHO怎么分级
乳腺癌是女性常见疾病,乳腺癌的发病与遗传、饮食、辐射、生活方式等因素有关。近几年乳腺癌的发病率增高,给女性朋友带来大的伤害。为女性乳房健康,一定要对乳腺癌早期治疗效果,在治疗乳腺癌之前,先要了解 乳腺癌的分级与分期, 才能对症治疗。
乳腺癌的分级与分期一、经典的TNM分期。
基本架构是根据肿瘤大小(简称T),淋巴结是否转移及转移数目(简称N),及是否有远处器官转移(简称M)等三者综合分析TNM以决定乳癌的分期。TNM这种肿瘤解剖病理分期对于预测肿瘤的复发转移价值不可低估,是临床上较成熟的风险评估指标。
原发肿瘤(T)分期:Tx 原发肿瘤情况不详(已被切除)。T0 原发肿瘤未扪及。Tis 原位癌(包括小叶原位癌及导管内癌),Paget病局限于乳头,乳房内未扪及块物。T1 肿瘤最大径小于2Cm。T2 肿瘤最大径2~5crn。T3 肿瘤最大径超过125px。T4 肿瘤任何大小,直接侵犯胸壁和皮肤(包括炎性乳腺癌)。
区域淋巴结(N)分期:N0 区域淋巴结未扪及。Nx 区域淋巴结情况不详(以往已切除)。N1 同侧腋淋巴结有肿大,可以活动。N2 同侧腋淋巴结肿大,互相融合,或与其他组织粘连。N3 同侧内乳淋巴结有转移、同侧锁骨下、上淋巴结转移。
远处转移(M)分期:Mx 有无远处转移不详。M0 无远处转移。M1 远处转移。
二、实用的临床分期。
根据不同的TNM可以组成临床不同分期,也是临床医生向患者及家属解释病情最常用的分期。
三、病理学分类、组织学分级。
乳腺癌病理组织形态较为复杂,类型众多,而且往往在同一块癌组织中,甚至同一张切片内可有两种以上类型同时存在。每种类型乳腺癌综合治疗方法及预后不同,临床制定治疗方案亦需结合病理类型及组织学分级。目前国际、国内的乳癌病理分类,在实际应用中仍未统一。
(一)目前国内多用以下病理分类。
1、非浸润性癌。
①导管内癌(癌细胞未突破导管壁基底膜);
②小叶原位癌(癌细胞未突破末梢乳管或腺泡基底膜);
③导管内乳头状癌;
④乳头样乳腺癌。此型属早期,预后较好。
2、早期浸润性癌。
①早期浸润性导管癌(癌细胞突破管壁基底膜,开始向间质浸润);
②早期浸润性小叶癌(癌细胞突破末梢乳管或腺泡基底膜,开始向间质浸润,但仍局限于小叶内)。此型仍属早期,预后较好。(早期浸润是指癌的浸润成分小于l0%)。
3、浸润性癌。
(1)浸润性特殊癌:乳头状癌、髓样癌(伴大量淋巴细胞浸润)、小管癌(高分化腺癌)、腺样囊性癌、粘液腺癌、大汗腺样癌、鳞状细胞癌等。此型分化一般较高,预后尚好。
(2)浸润性非特殊癌:包括浸润性导管癌(临床上最为常见类型)、浸润性小叶癌、硬癌、髓样癌(无大量淋巴细胞浸润)、单纯癌、腺癌等。此型一般分化低,预后较上述类型差,且是乳腺癌中最常见的类型,占80%,但判断预后尚需结合疾病分期等因素。
4、其它罕见癌。
(二)组织学分级标准。
肿瘤的组织学分级与患者预后的关系早已引起肿瘤学家的重视。乳腺癌的分化程度与预后有十分密切的关系,但各种分级标准的差异颇大。乳腺癌组织学分级主要从以下3个方面进行评估:
1、腺管形成的程度。
2、细胞核的多形性。
3、核分裂计数。
我国常见恶性肿瘤诊治规范的分级标准:
1、腺管形成 :①有多数明显腺管为1分。 ②有中度分化腺管为2分。③细胞呈实性片块或条索状生长为3分。
2、细胞核大小、形状及染色质不规则 ①细胞核大小、形状及染色质一致为1分。 ②细胞核中度不规则为2分。③细胞核明显多形性为3分。
3、染色质增多及核分裂相(?400) ①1/10HPF为1分。②2~3/10HPF为2分。③>3/10HPF为3分。
各标准的3项指标所确定的分数相加,3~5分为I级(分化好),6~7分为Ⅱ级(中等分化),8~9分为Ⅲ级(分化差)。
四、分子分型(以基因水平为基础的新分类)。
近年来,基于DNA微阵列技术和多基因RT-PCR定量检测的方法对乳腺癌进行的分子分型来预测乳腺癌的复发转移风险及其对治疗的反应,目前常将基因芯片技术的分子亚型和免疫组织化学结合起来,临床上可将乳腺癌划分为4类[55-57]:Luminal A 型 (ER+/PR+,HER-2-) 、Luminal B 型 (ER+/PR+,HER-2+)、HER-2+ 型 (ER-/PR-/HER-2+)和Basal-like型 (ER-/PR-/HER-2-)。不同分子亚型乳腺癌的临床治疗反应和生存期不同,目前越来越来引起临床重视。
五、危险度分级 (2007 St、 Gallen共识)。
根据患者年龄、肿瘤大小、激素受体状态、肿瘤细胞分级、脉管瘤栓、HER2状态、淋巴结状态,2007年St、Gallen专家共识将其分为低、中、高危复发风险人群,为临床医师选择合适的治疗方案提供了依据。
乳房疾病 乳腺癌的原因乳腺癌的病因一:
月经初潮早绝经晚。月经初潮年龄小于12岁与大于17岁相比,乳腺癌发生的相对危险增加2.2倍。闭经年龄大于55岁比小于45岁者发生乳腺癌的危险性增加1倍。月经初潮早,绝经晚是乳腺癌最主要的两个危险因素。
乳腺癌的病因二:
遗传因素。有研究发现,如果其母亲在绝经前曾患双侧乳癌的妇女,自身患乳腺癌的危险性为一般妇女的9倍,而且乳腺癌病人的第二代出现乳腺癌的平均年龄约比一般人提早10年左右。姐妹当中有患乳癌的女性,危险性为常人的3倍。需要强调的是,乳腺癌并不是直接遗传,而是一种?癌症素质?的遗传,乳腺癌病人的亲属并非一定患乳腺癌,只是比一般人患乳腺癌的可能性要大。
乳腺癌的病因三:
婚育。流行病学研究表明,女性虽婚而不育或第一胎在30岁以后亦为不利因素,但未婚者发生乳癌的危险为婚者的2倍。专家认为,生育对乳腺有保护作用,但仅指在30岁以前有足月产者。近年来的研究认为,哺乳对乳腺癌的发生有保护作用,主要是对绝经前的妇女。
乳腺癌的病因四:
电离辐射。乳腺是对电离辐射致癌活性较敏感的组织。年轻时为乳腺有丝分裂活动阶段,对电离辐射致癌效应最敏感,而电离辐射的效应有累加性,多次小剂量暴露与一次大剂量暴露的危险程度相同,具有剂量-效应关系。
乳腺癌的病因五:
不健康的饮食习惯。乳腺癌的发病率和死亡率与人均消化脂肪量有较强的相关。有些公司职员高收入造成高生活水准,形成不科学的、不健康的?高热量、高脂肪?饮食习惯,结果导致乳腺癌的发病率大大提高。
乳腺癌的病因六:
不健康的生活方式。有些长期从事办公室工作的女性白领坐多动少,缺乏锻炼,接触阳光少。大多职业女性由于工作关系,长时间紧箍着乳罩,难得给乳腺?松绑?;还有些职业女性迫于工作的压力或追求事业的成功,过着单身贵族或丁克族生活,不成家,不要孩子。
精彩推荐:
脖子上长小肉疙瘩 黑枸杞的功效与作用 女性健康生活小常识 洋葱泡红酒 螃蟹怎么洗 拔罐减肥 淡菜怎么洗 脚后跟疼 白醋泡脚?
乳腺癌组织学分级和病理分期
肿瘤的组织学分级与患者预后的关系早已引起肿瘤学家的重视。乳腺癌的分化程度与预后有十分密切的关系,但各种分级标准的差异颇大。乳腺癌组织学分级主要从以下3个方面进行评估。1.腺管形成的程度。
2.细胞核的多形性。
3.核分裂计数。
以下为不同的分级标准:
A. SBR分级标准
1.分化程度估计 根据形成腺管或乳头的能力:①整个肿瘤可看到为1分。②不容易发现为3分。③1分与3分之间为2分。
2.多形性①核规则、类似乳腺上皮为1分。②核明显不规则,有巨核、畸形核为3分。③1分与3分之间为2分。
3.核分裂数(×400) ①1/10HPF为1分。②2/10HPF为2分。③>2/10HPF为3分。
B.WHO分级标准
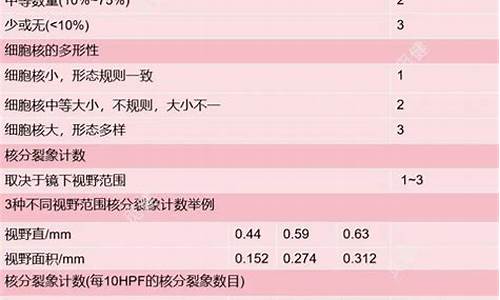
1.腺管形成 ①>75%为1分。②10%~75%为2分。③<10%为3分。
2.核的多形性①核小、规则、形态一致为1分。②核的形状、大小有中等度的变化为2分。③核的形状、大小有明显变化为3分。
3.核分裂数(×400)①0~5/10HPF为1分。②6~10/10HPF为2分。③>11/10HPF为3分。
C. 我国常见恶性肿瘤诊治规范的分级标准
1.腺管形成 有多数明显腺管为1分。②有中度分化腺管为2分。③细胞呈实性片块或条索状生长为3分。
2.细胞核大小、形状及染色质不规则 ①细胞核大小、形状及染色质一致为1分。②细胞核中度不规则为2分。③细胞核明显多形性为3分。
3.染色质增多及核分裂相(×400) ①1/10HPF为1分。②2~3/10HPF为2分。③>3/10HPF为3分。
各标准的3项指标所确定的分数相加,3~5分为I级(分化好),6~7分为Ⅱ级(中等分化),8~9分为Ⅲ级(分化差)。
乳腺癌组织学分级的意义
乳腺癌组织学分级的预后意义早为大家所认识。我们对有5年以上随访的476例乳腺癌患者进行了分级研究,其结果是组织学分级和生存情况为I级、Ⅱ级和Ⅲ级的5年生存率分别是82%、63.4%和49.5%,其差别有显著性意义(P<0.0l)。在同一临床分期内,患者的5年生存率随着组织学分级的提高而下降。
组织学分级与DNA增殖指数和DNA倍体有关,分化好的乳腺癌增殖指数低,反之分化差的增殖指数高。利用流式细胞证实了二倍体的乳腺癌,常常是分化好的,而异倍体的乳腺癌常常是分化差的。组织学分级和生长因子受体、癌基因产物的表达也有关,Ⅲ级乳腺癌常有上皮生长因子受体的表达,提示预后差,某些癌基因产物如c—erbB2的表达提示患者预后较差,常在Ⅲ级乳腺癌中表达。
乳腺癌的组织学分级和组织学分型均为影响乳腺癌预后的病理因素,两者中组织学分级型对判断患者的预后更有意义。
虽然组织学分级和分型均为独立的预后因素,但淋巴结有无转移、肿瘤大小更是影响患者预后的重要因素。1982年,Ilaybiffle和Elston等认为与预后有关的3个因素是①肿瘤大小(病理测量)、②组织学的淋巴结分期和③组织学分级,并在cox分析中得出预后指数的公式:预后指数=0.2×肿瘤大小+淋巴结分期+组织学分级,预后指数增高的患者预后差,以后多量的病例分析也证实了他们的论点。
乳腺癌的临床分期
0期:同侧腋窝未扪及淋巴结,肿瘤直径小于2cm
Ⅰ期:同侧腋窝扪及活动淋巴结,有或无转移,肿瘤直径2~5cm
Ⅱ期:同侧腋窝淋巴结融合成块与其它组织粘连,肿瘤直径大于5cm
Ⅲ期:同侧锁骨上、下或腋窝淋巴结内有转移或上肢水肿。转移淋巴结融合且硬
Ⅳ期:远处其它部位有转移
病理学分类(pTNM)
T 原发肿瘤
TX 原发肿瘤无法确定(例如已切除)
T0 原发肿瘤未查出
Tis 原位癌
Tis(DCIS) 导管原位癌
Tis(LCIS) 小叶原位癌
Tis(Paget) 不伴肿瘤的乳头派杰氏病
注:伴有肿块的派杰氏病根据肿块大小进行分期
T1 肿瘤最大直径≤2cm
T1mic 微小浸润性癌,最大直径≤0.1cm
T1a 最大直径>0.1cm,≤0.5cm
T1b 最大直径>0.5cm,≤1.0cm
T1c 最大直径>1.0cm,≤2.0cm
T2 最大直径>2.0cm,≤5.0cm
T3 最大直径>5.0cm
T4 不论肿瘤大小,直接侵犯胸壁或皮肤(胸壁包括肋骨、肋间肌、前锯肌,但不包括胸肌)
T4a 侵犯胸壁
T4b 患侧乳房皮肤水肿(包括桔皮样变),溃疡或卫星状结节
T4c T4a和T4b并存
T4d 炎性乳腺癌
N 区域淋巴结
Nx 区域淋巴结无法分析(例如已清除)
N0 区域淋巴结无转移
N1 同侧腋淋巴结转移,可活动
N2 同侧腋淋巴结相互融合,或与其他组织固定;或临床无证据显示腋淋巴结转移的情况下,存在临床明显的内乳淋巴结转移
N2a 同侧腋淋巴结相互融合,或与其他组织固定
N2b 临床无证据显示腋淋巴结转移的情况下,存在临床明显的内乳淋巴结转移
N3 同侧锁骨下淋巴结转移;或有临床证据显示腋淋巴结转移的情况下,存在临床明显的内乳淋巴结转移;或同侧锁骨上淋巴结转移,伴或不伴腋淋巴结或内乳淋巴结转移
N3a 同侧锁骨下淋巴结转移及腋淋巴结转移
N3b 同侧内乳淋巴结及腋淋巴结转移
N3c 同侧锁骨上淋巴结转移
pN 区域淋巴结
pNx 区域淋巴结无法分析(手术未包括该部位或过去已切除)
pN0 组织学无区域淋巴结转移,未对孤立肿瘤细胞另行检查
pN0(i-) 组织学无区域淋巴结转移,免疫组化阴性
pN0(i+) 组织学无区域淋巴结转移,免疫组化阳性,肿瘤灶≤0.2mm
pN0(mol-)组织学无区域淋巴结转移,分子检测(RT-PCR)阴性
pN0(mol+)组织学无区域淋巴结转移,分子检测(RT-PCR)阳性
pN1mi 存在微转移,最大径>0.2mm,≤2.0mm
pN1 同侧1~3个腋淋巴结转移,或内乳前哨淋巴结镜下转移,而临床不明显
pN1a 同侧1~3个腋淋巴结转移
pN1b 内乳前哨淋巴结镜下转移,而临床不明显
pN1c 同侧1~3个腋淋巴结转移,同侧内乳前哨淋巴结镜下转移,而临床不明显
pN2 4~9个腋淋巴结转移,或临床明显的内乳淋巴结转移而腋淋巴结无转移
pN2a 4~9个腋淋巴结转移,至少一个肿瘤灶>2.0mm
pN2b 临床明显的内乳淋巴结转移而腋淋巴结无转移
pN3 10个或10个以上腋淋巴结转移,或锁骨下淋巴结转移,或腋淋巴结转移的情况下伴临床明显的同侧内乳淋巴结转移;或3个以上腋淋巴结转移伴有临床阴性而镜下内乳淋巴结转移;或同侧锁骨上淋巴结转移
pN3a 10个或10个以上腋淋巴结转移(至少一个肿瘤灶>2.0mm),或锁骨下淋巴结转移
pN3b 3个以上腋淋巴结转移伴有临床阴性而前哨淋巴结活检镜下内乳淋巴结转移
pN3c 同侧锁骨上淋巴结转移
M 远处转移
Mx 有无远处转移无法评估
M0 无远处转移
M1 有远处转移
说明:
临床明显:指通过临床体检或影像学检查(除外淋巴核素显象)发现;
pN分类依据腋淋巴结清扫结果,此前可有、可无前哨淋巴结活检,如果只进行前哨淋巴结活检而其后未行腋淋巴结清扫,以(sn)表示前哨淋巴结,如pN0(i+)(sn);
孤立肿瘤细胞指单个细胞或小于0.2mm的小细胞团,通常由免疫组化或分子技术发现,并经常规组织学鉴定,孤立肿瘤细胞不一定显示转移活性,如增殖或间质反应。
临床不明显:指临床体检或影像学检查(除外淋巴核素显象)不能发现的情况。
临床分期
O期 Tis N0 M0
I 期 T1 N0 M0
IIA期 T0 N1 M0
T1 N1 M0
T2 N0 M0
IIB期 T2 N1 M0
T3 N0 M0
IIIA期 T0 N2 M0
T1 N2 M0
T2 N2 M0
T3 N1~2 M0
IIIB期 T4 N0 M0
T4 N1 M0
T4 N2 M0
IIIC期 任何T N3 M0
IV期 任何T 任何N M1
组织病理学分级(G)
Gx 不能判断分化程度。
G1 高分化。
G2 中度分化。
G3 低分化。
手术治疗后有无残存瘤情况分类(R)
Rx 无法肯定有无残存瘤。
R0 无残存瘤。
R1 镜下可见残存瘤。
R2 肉眼可见残存瘤。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。












